
创新药研发周期平均需7.2年,参加新药临床试验几乎是提前使用新药的主要途径
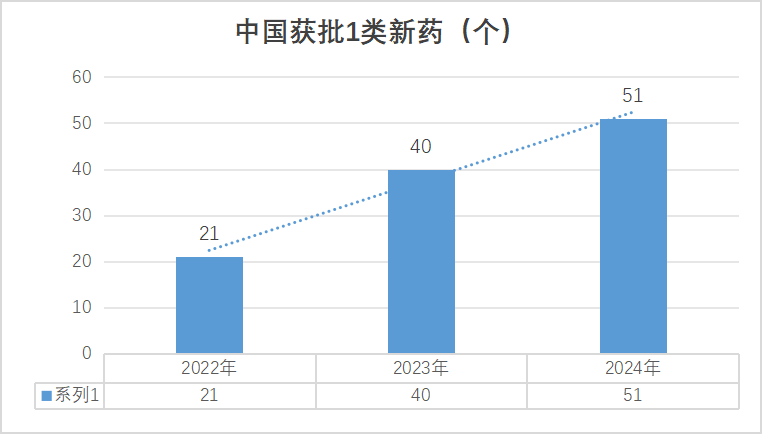
近3年110+款1类创新药在中国获批,呈逐年递增趋势。其中2022年有21款,2023年有40款1类新药,2024年约有50款+。[1-3]涉及的领域覆盖了肿瘤,如肺癌,乳腺癌,胃癌,多发性骨髓瘤等;常见病,如阿尔茨海默病,2型糖尿病,高血脂,特应性皮炎,银屑病等;以及多个罕见疾病,如阵发性睡眠性血红蛋白尿症,杜氏肌营养不良症等。填补了多个治疗领域空白,为众多患者带来了治疗的希望和新的治疗选择。
亮点有:
1.中国迎来20年来首款获得FDA完全批准的阿尔茨海默病(AD)新疗法仑卡奈单抗,为早期阿尔茨海默病早诊早治提供“对因”治疗药物。
2.全球首个针对糖尿病黄斑水肿的VEGF-A/ANG-2双抗法瑞西单抗中国获批,为糖尿病黄斑水肿患者带来更多治疗选择。
3.每周一次超长效胰岛素依柯胰岛素中国获批,显著缩短给药周期,为糖尿病患者用药带来更便捷的治疗药物。
4.全球首个针对肺癌脑转移的EGFR-TKI新药盐酸佐利替尼片获批,为肺癌脑转移患者带来针对性治疗药物;
5.中国首个KRAS G12C抑制剂氟泽雷塞获批,为KRAS G12C突变型晚期非小细胞肺癌(NSCLC)带来针对性靶向治疗;
6.全球首创新药注射用利纳西普填补罕见病冷吡啉相关周期性综合征治疗空白;
。。。。。。
什么是1类创新药?
1类创新药是指尚未在国内外上市的药,含有新的结构明确的、具有药理作用的化合物或生物制品,且具有临床价值的药品。
创新药的获批为我们带来了什么?
- 填补了该领域治疗空白,如某些罕见疾病不再无药可治,某些肿瘤特定靶点有了新药,迎来针对性治疗药物;
2)带来更优疗效,更便捷的治疗方式,副作用更低等;
3)为患者提供更多治疗选择。

创新药批准上市需要多久?
根据《中国新药注册临床试验进展年度报告 (2023年)》显示,2023 年度创新药获准上市所用时间平均为 7.2 年。[4]这个时间是从批准开展临床试验到批准上市的平均时长,部分药物由于各种因素的影响,从批准临床试验到获批上市花费时间可能会长达10年,甚至更久。新药获批需要等待数年,但一旦获批,将为无数的患者带来新的治疗选择,或是填补治疗空白,或是带来更优治疗选择。。。。。。
新药研发周期平均需7.2年,我如何更早的使用到新药?
新药研发之路漫且长,即使经历数年获批上市,到我们能真正使用到药物依旧需要等待。当我们亟需使用新药,寻求新的治疗选择时,或许新药临床试验能为我们开辟一条“捷径”让我们有机会提前使用新药。

为什么国外已经上市的药中国还需要做临床试验?
国外已经上市的药物,虽然对国外患者人群有较好的疗效和安全性,但由于人种的差异,还需要补充中国人群的用药数据来进一步证实该药同样对中国人群有效和安全,而临床试验是佐证新药疗效和安全的唯一途径。因此,大多情况下,国外已上市的新药还需要在国内进一步完成临床试验后才能上市。
为什么我的主治医生会建议我参加新药临床试验?
除了当前已经获批的药物,为了获得更优疗效和安全性的药物,保持医学的进步,新药的研发从未停止。
而对于当前治疗药物控制不佳或缺乏其它治疗选择或经济有限的患者来说,在保障患者权益的前提下,主治医生会将新药临床试验作为一种治疗方式推荐给患者。另外,国内外各大权威指南也将参加临床试验作为一种治疗方式进行推荐。

患者参加新药临床试验,一方面多了一种治疗选择,另一方面也能在新药研究中获得研究相关的检查和疾病管理,且能减轻患者的经济负担。
国际权威指南建议患者参加临床试验,从临床试验中获得新药治疗
美国国立综合癌症网络(NCCN)和中国肿瘤协会(CSCO)最新指南均推荐参加新药临床。NCCN认为任何癌症患者都可以在临床试验中得到最佳治疗,因此特别鼓励患者参与临床试验。

《以临床价值为导向的抗肿瘤药物临床研发指导原则》中明确提出:“对于晚期肿瘤患者而言,参与临床试验本身就是治疗手段之一”。国内外权威指南,无论是中国的CSCO指南、还是国外的NCCN指南、ASCO指南、ESMO指南,均推荐肿瘤患者积极参加临床研究。
我参加新药临床试验会不会错过最佳治疗?
国家药监局相继发布“以患者为中心的临床试验”相关治疗原则,试验设计中推荐选择对于受试者最佳的对照治疗,保障受试者权益。

临床试验是我们接触新药最早的途径,现在的研究新药很可能就是未来的标准治疗
武汉大学中心医院官网于2023年4月发布的文章[8]提及,在国外,很多患者会主动询问医生是否有适合他们的临床试验可以参加。世界范围内影响力最大的美国MD Anderson肿瘤中心有超过90%的患者参加临床试验,这也是美国肿瘤患者生存期长的原因之一。现在的临床研究很可能就是未来的标准治疗。
我在哪里可以看到新药临床试验信息?
因新药临床试验需要更专业的医院和医生去完成,因此新药临床试验通常集中在一、二线城市知名三甲医院。而很多患者因接触不到这些临床试验,错失了知晓和参与新药临床试验的机会。
联结患者与希望—————专业临床试验患者招募平台:新药之光小程序
为满足大众对各领域新药临床试验信息的需求,联结患者与希望,新药之光作为一个专业临床试验患者招募平台整合了各领域新药临床试验信息,让我们通过一键搜索直达疾病领域新药信息。新药之光目前覆盖的领域包含了常见疾病,肿瘤,罕见病,医美等多个领域新药临床信息,报名后我们可实时查询报名和参与临床试验的状态。
联结患者与希望,点亮新药之光,我们一起努力!
参考资料:
1.2023年药品审评报告.
2.2022年药品审评报告.
3.国家药监局官网:https://www.nmpa.gov.cn/
4.中国新药注册临床试验进展年度报告 (2023年)
5.中国晚期乳腺癌规范诊疗指南(2024版).
6.NCCN临床实践指南:非小细胞肺癌V3 2023.
7.以患者为中心的药物临床试验设计技术指导原则(试行).
8.武汉市中心医院.肿瘤患者参加临床试验是当“小白鼠”了吗?2023年4月.
https://www.zxhospital.com/zlk/info/1021/1703.htm

